設備(装置)の再バリデーションの実施内容の考え方 ~ 第647号 ~
設備(装置)の再バリデーションはなにをやるの?
> 前回、「設備(装置)の再バリデーションの時期(タイミング)の考え方」についてお届けしました。今回は、その続きとして「設備(装置)」の再バリデーションは具体的になにをどのように実施したらよいのか?ついて考えてみたいと思います。
まずは、規格の要求から確認してみたいと思います。

規格の「再バリデーション」の定義を調べてみました
> 「GMP省令」では「再バリデーション」は以下のように定義されています。
■ GMP省令
④ 再バリデーション
設備、装置若しくはシステム、製造工程、洗浄作業又は試験検査の方法が、据付時に検証され、管理された状態を維持している旨を再確認するため、定期的に適格性評価、プロセスバリデーション又は洗浄バリデーションを行う。
再バリデーションを行う必要性、時期(タイミング)及び項目については、その設備、装置若しくはシステム、製造工程、洗浄作業又は試験検査に係る製品の製造頻度のほか、医薬品に係る製品にあってはGMP省令第11条の2第1項第4号及び第21条の2第1項第4号の規定による安定性モタリングの評価、同令第11条の3第1項第1の定による製品品質の照査等の結果を踏まえ、製造業者等が定めるものであること。なお、例えば、無菌性保証のための培地充填試験のように、製品品質に大きな影響を及ぼす設備、装置若しくはシステム、製造工程、洗浄作業又は試験検査方法について検証する再バリデーションは、製品品質の照査等の結果によらず、定期的に行うことが求められる。
医薬品及び医薬部外品の製造管理及び品質管理の基準に関する省令の一部改正について(薬生監麻発0428第2号令和3年4月28日)
上記、GMP省令をみると、
「再バリデーション」は「予測的バリデーション」などの既に実施済のバリデーションの再確認のために実施するバリデーションであることや、そのために「適格性評価」「プロセスバリデーション」「洗浄バリデーション」を定期的に行うことが記載されています。
しかし、なにをどのように実施したらよいのか?については「必要性」「時期(タイミング)」「項目」などは製造業者が定めるものとされ、具体的に書かれていません。
そこが悩みところではないでしょうか?
設備(装置)の再バリデーションの実施内容の考え方(一例)
> 再バリデーションは最小で「付帯する計測器のキャリブレーション(校正)」、最大で「予測的バリデーションと同じ」になると考えます。
「付帯する計測器のキャリブレーション(校正)」をITEM1、「予測的バリデーションと同じ」をITEM3などと作業分類でタグ付けして、「構造設備の視点によるリスクアセスメントの一例」として下図にしてみました。
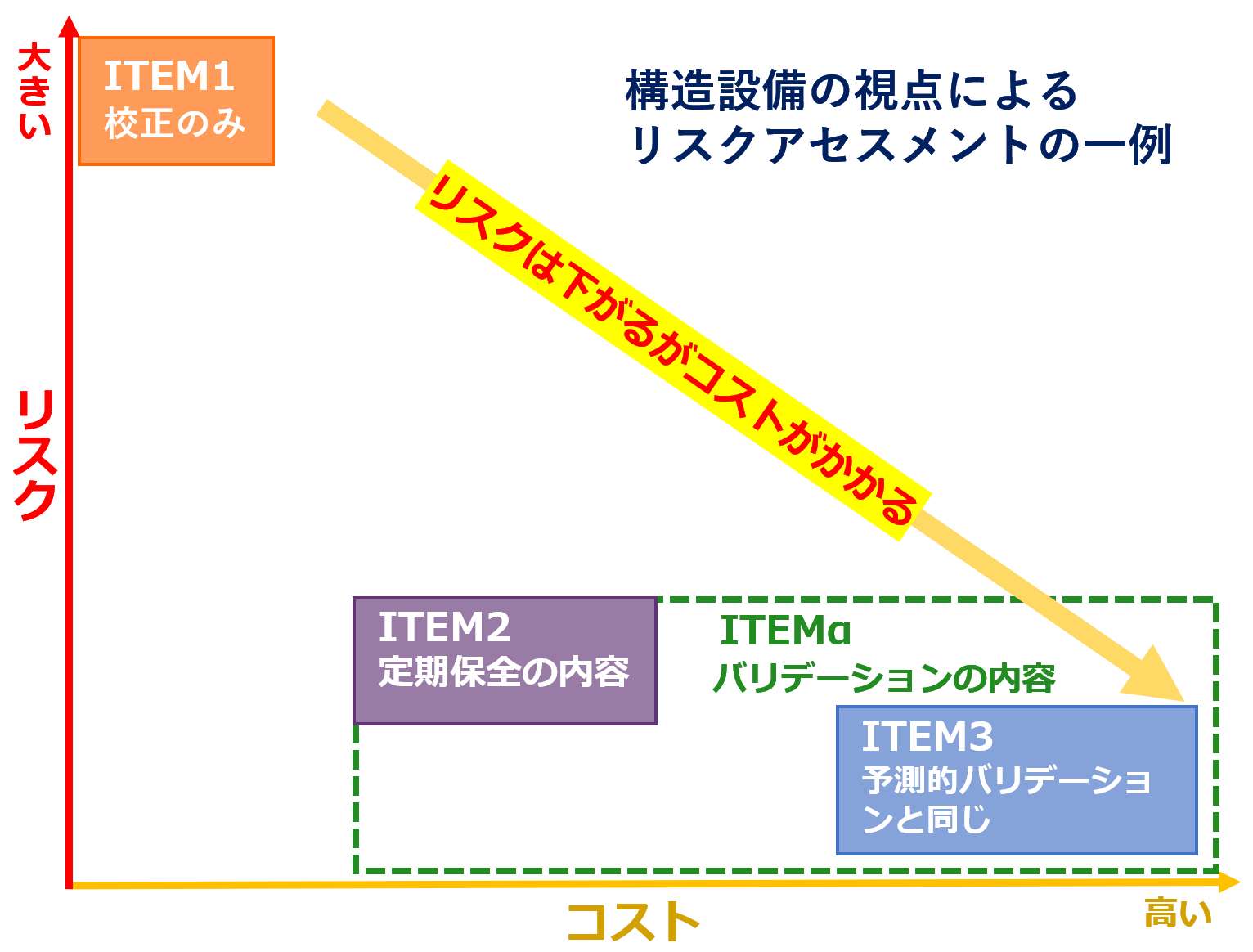
■ 作業分類した「ITEM1」「ITEM2」「ITEM3」「ITEMα」の説明は以下の通りです。
ITEM1:付帯する計測器のキャリブレーション(校正)
設備・装置に付帯する計測器のキャリブレーション(校正)は、その設備・装置の評価の為の基準となるため定期的な実施が必須と考えます。
なお、計測器の正しさは担保されますが、設備・装置の妥当性の担保は難しいと考えます。
ITEM2:「定期保全」での内容をリスクアセスメント
定期保全の内容、具体的には「部品交換」「オーバーホール」「調整」「洗浄・クリーニング」などの影響範囲(製品品質・プロセス運転・安全/環境など)を踏まえて「再バリデーション」する対象、内容を決定し実施します。
なお、リスクアセスメントの結果、GMPハードだけが対象であればPIC/S GMPガイドラインの「再クオリフィケーション(再適格性評価)」となると考えます。
ITEM3:予測的バリデーションと同じ
リスクに基づく評価をしながらも、事象や評価に関係なく定期的な「再バリデーション」を実施する考え方もあると思います。
ITEMα:予測的バリデーションの内容の変更有無とリスクアセスメント
実生産上、よりよい手順やよりよい設定により製品品質や生産量の改善を図る事があります。
この変更による影響範囲(製品品質・プロセス運転・安全/環境など)を踏まえて「再バリデーション」する対象、内容を決定し実施します。
なお、リスクアセスメントの結果、GMPハードだけが対象であれば、ITEM2とほぼ同じとなり、GMPハードおよびGMPソフトの両方が対象であればITEM3とほぼ同じになります。
再バリデーションの実施内容はITEMの組合せによって考えます
> 再バリデーションの実施内容は「リスクとコストの最適化」や「項目(内容)の明確化」のため、作業分類したITEMの組合せによって考えると良いと思います。
事例1:恒温恒湿槽 【ITEM1+ITEM2を実施】
ITEM1:付帯する計測器(温度計/湿度計/記録計など)
⇒(1年毎)キャリブレーション(校正)を実施
ITEM2:「定期保全(3年計画)」で記録計の「マルチプレクサ&センサー交換」
⇒ IOQ実施(再クオリフィケーション)
事例2:空調機システム 【ITEM1+ITEM2を実施】
ITEM1:付帯する計測器(温度計/湿度計/記録計など)
⇒(1年毎)キャリブレーション(校正)を実施
ITEM2:「定期保全(2年計画)」で「フィルター交換」
⇒ IOQ実施(再クオリフィケーション)
事例3:真空乳化装置 【ITEM1+ITEMαを実施】
ITEM1:付帯する計測器(温度計/圧力計/回転計/記録計など)
⇒(1年毎)キャリブレーション(校正)を実施
ITEMα:「対象医療品変更」で「研究棟Aから研究棟Bに移動」
⇒ IQ/OQ/PQ/PV実施(予測的バリデーションと同じ)
⇒ ここでは設備(装置)の視点で一つの考え方を示しました。
リスクとコストのバランスを考えながら「再バリデーション」でなにをどのように実施していくのか、それぞれの現場に合った最適な方法を考えてみてはいかがでしょうか。
▼ 「再バリデーション」についても「無料オンライン相談会」からご相談していただくこともできます。
※ 当社は、フィールドでバリデーション・キャリブレーションを実施する立場から、規格の要求内容や定義を具体化(具現化)して、お客様に満足して頂ける作業をお届けする努力を続けています。
最後まで、お読みいただき有難うございました。

