第569号 バリデーションにおける校正(キャリブレーション)実施要求の移り変わり

3つ前のGMP省令まで振り返り、校正要求の移り変わりをご紹介します
> 8/1に施行された改正GMP省令では校正のタイミングはどんな感じの記載になっているのでしょうか
その点に注目して、過去からの移り変わりを調べてみました。
平成7年の[旧]バリデーション基準では、バリデーション実施時に校正をどのタイミングで実施したらよいか分かり易い記載になっていました。
■ 平成7年に発布された[旧]バリデーション基準での要求

このように、校正は「1設備の据付時における設備の適格性の確認」と「3稼働性能適格性の確認」の間で実施すれば良いことが明確になっていました。
平成25年の[前]バリデーション基準では校正要求は分かりにくくなった
> 平成25年8月30日に発布された「医薬品及び医薬部外品の製造管理及び品質管理の基準に関する省令の取扱いについて」での[前]バリデーション基準には、校正のタイミングが明記されていません。
■ 校正に関わる要求は

としか記載されていません。
これでは、何をどのタイミングで校正したら良いか分からないも頷けるとこです。
8/1に施行された改正GMP省令は分かり易い?
> 改正GMP省令は、2021年4月28日付けで、「医薬品及び医薬部外品の製造管理及び品質管理の基準に関する省令の一部を改正する省令」で公布され、同年8月1日に施行されました。
■ 校正に関わる要求

このように、IQ、OQ、PQの適格性評価において、「適切に校正を行った計測器を用いること」と要求されていて、平成25年の[前]バリデーション基準の校正要求とほぼ同じで校正のタイミングは明記されていません。
3つの規格の校正要求をイメージ図で表してみました
> 適格性評価の段階毎に分けて、校正がどこで要求されているか図式化してみました。
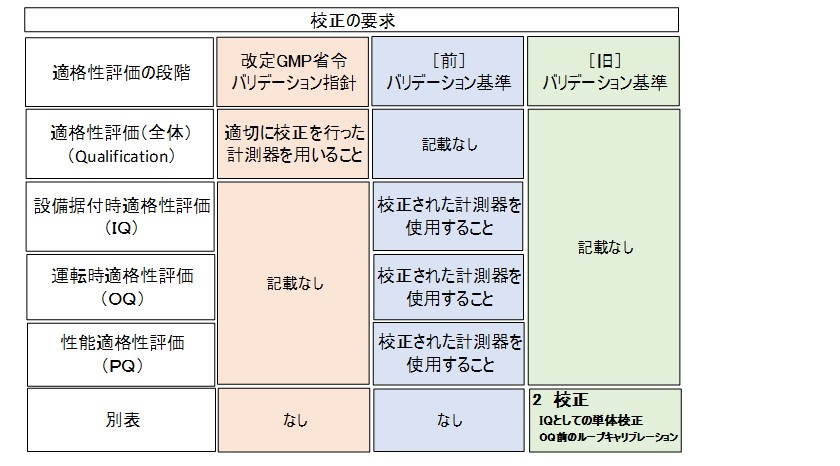
このイメージ図では、改定GMP省令のバリデーション指針の要求は、表現の仕方は[旧]バリデーション基準に、内容は[前]バリデーション基準に似ていると思います。
全体としては、[前][旧]のバリデーション基準の中間の表現なっていると感じています。
3つの規格とも、校正の考え方はほとんど変わらない
> 今回、3世代のGMP省令で調べた移り変わりでは、校正要求はほとんど違わないと
考えられます。
従って、校正については従来通り、2つの校正を実施することになると考えます。
①IQ・OQ・PQで使用する計測器の校正(JISの定義に基づく校正)
②設備・システム又は装置に付帯する計測器の校正(GMPの定義に基づく校正)
■ このように考えると、校正のタイミングは、IQ・OQ・PQ実施前に終わっておくと理解しておくのも良いかなと当社は考えています。
※ 当社は、フィールドでバリデーション・キャリブレーションを実施する立場から、規格の要求内容や定義を具体化(具現化)して、お客様に満足して頂ける作業をお届けする努力を続けています。
最後まで、お読みいただき有難うございました。
