第568号 改正GMP省令と改正前のGMP省令でのバリデーション(適格性評価)の相違点
令和3年8月1日に施行された改正GMP省令、細部まで確認してみると
> ご存知のように、2021年4月28日付けで、「医薬品及び医薬部外品の製造管理及び品質管理の基準に関する省令の一部を改正する省令」が公布され、同年8月1日に施行されました。
■ この改正GMP省令では、以下の記載のように、バリデーションについては大幅な改定になっていない様に思われます。

※ 今回は、細かい点においても、2つの省令でのバリデーションについての相違点が無いか調べてみることにしました。
2つの規格要求に小さな相違点が見つかりました
> 「改正GMP省令」と「改正前のGMP省令」の適格性評価の要求を並べてみました。
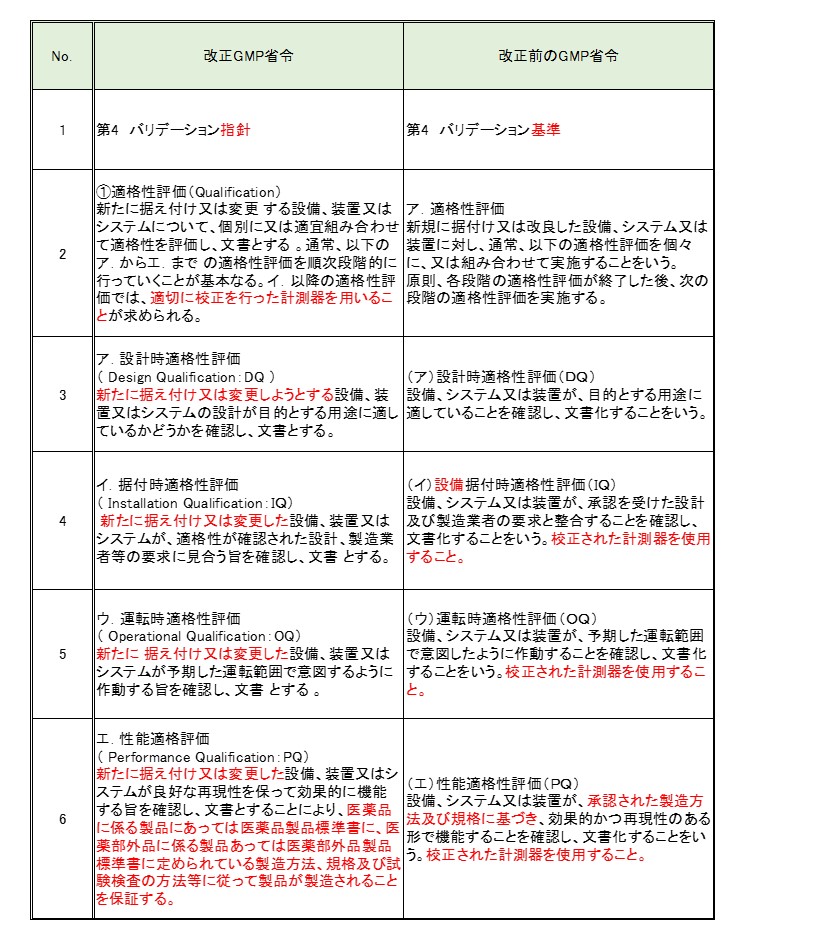
※ 2つの規格要求の相違点を「赤字」にしてみると、細かいところですが違いがあることが分かりました。
当然ですが、PIC/S GMP ガイドラインの考えが色濃く反映されている
> 両方の規格要求を並べて確認することで大きな変更がないことが分かりましたが、PIC/S GMP ガイドラインが色濃く反映されていると感じました。

こんなところからも、改正GMP省令の経緯と趣旨のGMP省令について、一層の国際整合を図る観点から本改正が行われたことが伺えました。
バリデーション(適格性評価)の現場作業は大きく変わらない?
> 今回行った両方の規格要求を並べて確認することでは、大きな変更がないことが分かりました。
従って、バリデーション(適格性評価)の現場作業は、実施内容や方法を大きく変更をしなくても良いと考えられますが、最終的にはバリデーション計画書の内容なども細かく確認して判断したいと考えています。
※ 当社は、フィールドでバリデーション・キャリブレーションを実施する立場から、規格の要求内容や定義を具体化(具現化)して、お客様に満足して頂ける作業をお届けする努力を続けています。
最後まで、お読みいただき有難うございました。
