第567号 PIC/S GMP ガイドラインとバリデーション基準の「プロセスバリデーション(PV)」を比較しました
プロセスバリデーション(PV)も、PIC/S GMP ガイドラインとバリデーション基準の要求に違いがあるのか
> ご存じの様に、バリデーション基準は、平成25年薬食監麻発0830第1号により全面改訂され、プロセスバリデーションの考え方の整備がされました。
今回ご紹介するプロセスバリデーション(PV)は以下のような考え方で整備されたと認識しています。

※ 当社では、このようなPVに関わることは多くありませんが、「PIC/S GMP ガイドライン」と「GMP省令のバリデーション基準」での規格上の相違点などを比較してご紹介します。
適格性評価とは、感じの違う比較表になりました
> 今回の比較で引用した資料は次の通りです。
□ PIC/S GMP ガイドラインは、平成27年7月8日事務連絡「PIC/SのGMPガイドラインを活用する際の考え方について」の一部改訂についてで発布されたアネックス15のクオリフィケーション及びバリデーションを引用しました。
□ バリデーション基準は、平成25年8月30日のGMP省令から引用しました。
【PIC/S GMP ガイドラインとバリデーション基準との比較】
■ PROCESS VALIDATION:プロセスバリデーション
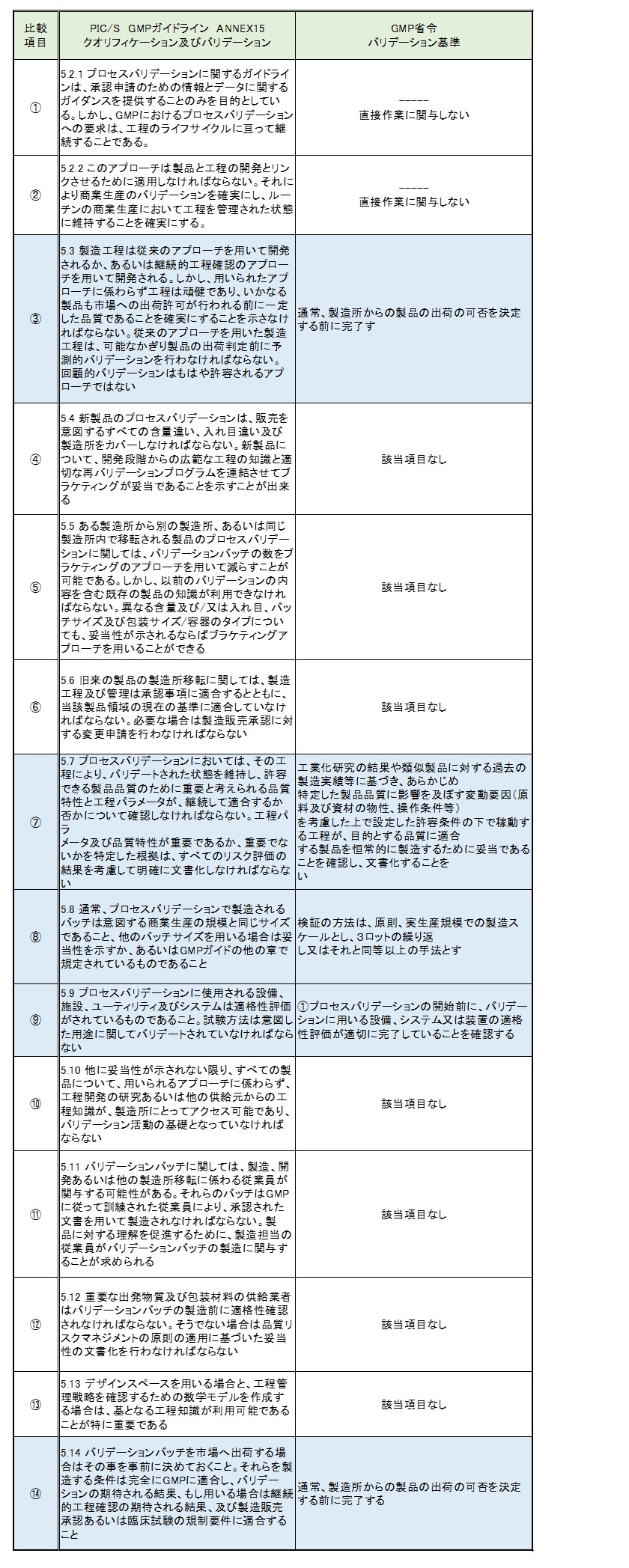
※ このように、PIC/S GMP ガイドラインには、今までの「DQ」「IQ」「OQ」「PQ」「計画書」の比較表と違いバリデーション基準に該当しない項目が多くあると思いました。
「該当項目なし」が多いのは、PVの重要性を分かり易くしている?
> 比較表において、該当項目なしが多い理由を、比較項目の内容から当社視点で考察してみるとプロセスバリデーションが重要な位置づけになっていることが伺えます。
例えば、
[比較項目①]では、GMPにおけるプロセスバリデーションへの要求は、工程のライフサイクルに亘って継続することである。
[比較項目②]では、商業生産のバリデーションを確実にし、ルーチンの商業生産において工程を管理された状態に維持することを確実にする。
など、リスクを排除しようとする強い意志が伝わってきました。
※ PIC/S GMP ガイドラインがリスクベースで考えられていること良く分かりました。
今後のGMPの考え方はリスクベース!
> 今更ですが、このような比較を続けてくるとリスクベースの考え方がより重要性が増していると考えられます。

■ 今後は、QMS省令のバリデーション基準などにおいても、PIC/S GMP ガイドライン等で求められるリスクベースアプローチは、このようなリスクベースの考え方も重要と考えられます。
※ 当社は、フィールドでバリデーション・キャリブレーションを実施する立場から、規格の要求内容や定義を具体化(具現化)して、お客様に満足して頂ける作業をお届けする努力を続けています。
最後まで、お読みいただき有難うございました。
