第554号 製薬設備のバリデーションは2つの規格をどのように実施するのか
製薬設備のバリデーションの2つの規格は二度手間になるのか
> 前回のメルマガから考えると、
コンピュータ化システムの製薬設備のバリデーションは、同じ設備でありながら、コンピュータ化システム適正管理ガイドラインの要求内容で実施し、バリデーション基準の要求内容でも実施することになります。
■ このような二度手間のような2つのバリデーションがあり混乱してしまいますので、今回はスッキリ整理するひとつの考え方をご紹介したいと思います。
※ まずは、GMPのバリデーション基準から考えることにしました。
コンピュータ化システムも製造所の構造設備のひとつ!
> GMP省令のバリデーション基準においては、バリデーションの目的を次の様に定めています。

⇒このように、バリデーション基準のバリデーションの目的では、製造所の構造設備自体が「コンピュータを使ったシステムか」「使っていないシステムか」は関係ないことが分かります。

コンピュータ化システム適正管理ガイドラインもまとめて実施しても良いと解説!
> コンピュータ化システム適正管理ガイドラインでは「性能適格性評価(PQ)の計画に関する文書の作成」を要求しています。
要求内容には「システムの稼働時における機能及び性能の確認方法」が求められ、この混乱を解決する考え方の解説があります。
■ 「システムの稼働時における機能及び性能の確認方法」の解説

文中の「システム」はコンピュータ化システム適正管理ガイドライン、「設備」は「バリデーション基準」と読み解けますので
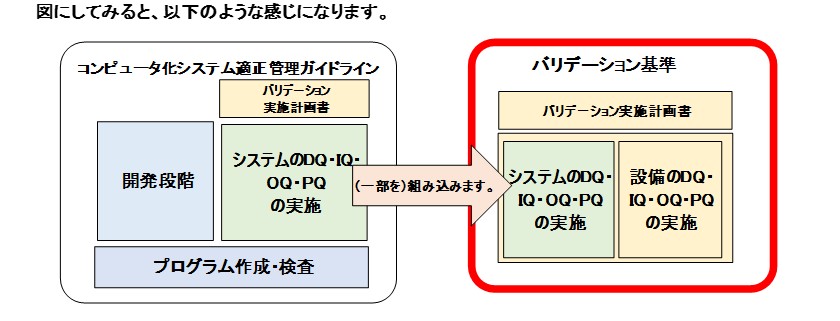
⇒二つの要求内容が違っていても、緑の部分が組み込まれていると考えると、整理が出来ます。
※ コンピュータ化システム適正管理ガイドラインにおけるバリデーションは、バリデーション基準のバリデーションの一部として実施して良いと考えられます。
結論は、バリデーション基準に組み込んで実施!
> ここまで調べた内容の結論をまとめました。

■ このように考えることで、どの規格でバリデーションを実施したらよいかの判断の助けになると思います。
※ 当社は、フィールドでバリデーション・キャリブレーションを実施する立場から、規格の要求内容や定義を具体化(具現化)して、お客様に満足して頂ける作業をお届けする努力を続けています。
最後まで、お読みいただき有難うございました。
